18日夜里,美国生物科创公司Moderna(NASDAQ:MRNA)公布了新冠病毒疫苗mRNA-1273早期人体试验数据:45位受试者全部产生抗体,最初8位产生了中和抗体,最小剂量(25微克)组在试验第43天时体内抗体水平与新冠肺炎痊愈者相当,而100微克组则“显著超过这一水平”,而且试验中没有出现严重的不良反应事件。
对于当前的疫情,疫苗有如“救世主”一般的存在。而疫苗拯救世界之前,昨晚先在股市预演了剧本。受试验积极数据影响,Moderna昨晚股价上涨近20%(今年以来已上涨超过300%),并带动全球股市上涨,疫情全球爆发之后一度下跌80%的邮轮公司,昨晚股价也上涨超过15%。
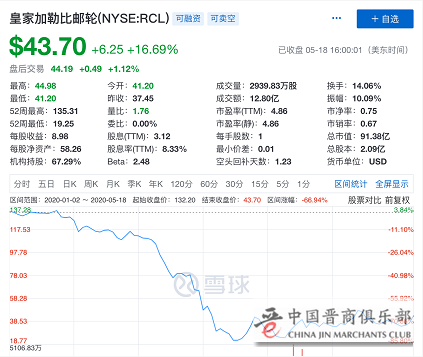
Moderna领跑新冠疫苗:
25微克就有效,副作用很小
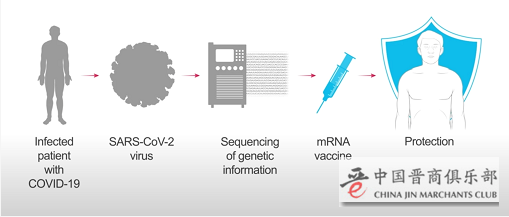
2020年1月10日,中国科学家上传了新型冠状病毒的全基因序列——一组拥有3万个“生化字母”的遗传密码。一万公里之外, Moderna下载了这串密码,并成为全球新冠疫苗研发的领跑者之一。3月16日,第一个进入临床试验, 4名志愿者在美国华盛顿州西雅图市接受了疫苗注射,一期试验共45位参与者。
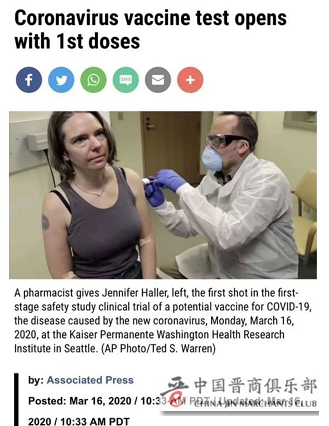
昨晚公布的结果,正是这45位志愿者者的数据。
根据试验安排,志愿者分为三个小组接受25微克、100微克和250微克的剂量注射,分别为15人、10人、20人。目前已经出炉的数据包含了25微克、100微克组接受两次注射后两周(共计43天),以及250微克组接受一次注射后29天的免疫数据。
根据公告,三种剂量在给药后15天都观察到免疫原性增加,在25 微克和100 微克剂量组,初次接种和加强接种之间均观察到增加。第二次注射后两周,25 微克组抗体达到新冠肺炎患者痊愈后的水平,100 微克剂量组则超过这一水平。
最初的8位受试者中(25 微克和100 微克剂量组各前四位),产生了中和抗体,中和抗体可有效阻止病毒感染细胞,被认为是对预防疾病有效的抗体。
试验中没有发现重大安全问题,mRNA-1273通常安全,且耐受性良好。在25 微克和100 微克剂量组中,只有一例3级不良反应,注射部位周围出现3级红斑。迄今为止,最明显的不良反应案例发生在250 微克剂量组的,但所有不良反应案例都是暂时性的,且可以自愈。

与NIAID合作的小鼠临床结果也一并发布。在这项研究中,mRNA-1273的疫苗接种可预防SARS-CoV-2在动物肺中的病毒复制。
“这些只是早期的第一阶段数据,但表明只接种25微克的mRNA-1273疫苗,也能在新冠病毒感染患者体内产生免疫反应,”Moderna首席医学官塔尔·扎克斯(Tal Zaks)说道:“结合此前开展成功的一项临床前挑战模型,这些数据证实了我们所相信的,即mRNA-1273疫苗具有预防新冠肺炎并为关键试验选择剂量的能力。”
根据第一阶段的数据, 第二阶段研究将修正为研究50 微克和100 微克两种剂量水平,以选择疫苗剂量。预计第三阶段研究的剂量在25 微克至100 微克之间,并预计7月份进行三期试验,具体取决于临床试验方案。
而根据此前报道,Moderna公司CEO斯蒂芬·班塞尔(Stephane Bancel)表示,疫苗最早将于7月开始批量生产,预计未来年产量能够达到10亿制剂。另外,FDA已授予这款疫苗快速通道认证资格,最早将于今年秋季推向医疗第一线。
新冠疫苗9月有望投入紧急使用
希望“拯救世界”的,不仅仅Moderna一家。
根据对Milken Institute数据的不完全统计,目前全世界新冠疫苗立项超过了130个,其中8个进入临床试验阶段,其中美国3个、英国1个,另外4个来自中国团队,包括康希诺(06185.HK)和军事科学院联合开发的腺病毒载体疫苗、科兴生物研发的灭活疫苗等等。
不过,临床试验到上市还有距离,通常情况下传统疫苗研发需要5~10年,新冠疫苗预计能缩短至12~18个月。而且疫苗研发成功率不高,近30年来美国FDA总共启动疫苗临床研究试验接近3000次,但是获批上市的疫苗的数量不足20个。而昨晚Moderna的数据公布后,投行高盛的分析师对其疫苗成功率的预测,是75%。
中国疾控中心主任高福4月23日在接受中国国际电视台采访时表示,中国处于新冠疫苗研发的前沿,在9月份可能有新冠疫苗投入紧急使用,例如再发生疫情时用于医护人员,预计明年年初可以用于健康人群。而根据此前的报道,Moderna、辉瑞和英国牛津大学团队的三款疫苗,能够投入使用的时间预期,也是9月左右。

5月15日,美国总统特朗普用了个科幻名字 “曲速计划 (Operation Warp Speed)”开启了美国的官方新冠疫苗加速计划。科幻作品里,曲速引擎是一种假想的超光速推进方式;而在现实中,美国政府在用政府、军方、私营单位的合力挑战疫苗开发、量产、普及的速度极限。这项斥资百亿美金被特朗普比喻为当代的曼哈顿核弹计划,期望锁定目前最优秀的疫苗项目,在2021年1月前完成三亿支新冠疫苗生产,覆盖全美人口。
但疫苗开发和生产并不是科幻电影,疫苗研发生产能否“超光速”还要遵循现实。
“疫苗拯救世界”联盟其他成员的进度
目前世界上新冠肺炎疫苗开发思路多样,包括灭活疫苗、减毒活疫苗、载体疫苗(复制性或非复制性)、病毒样颗粒、蛋白亚单位疫苗、以及比较新型的基因疫苗(DNA或RNA)等几个主要门类。单从立项来看,数量最多的是蛋白亚单位疫苗,约占总数三分之一。
进入临床试验阶段的8个项目 包括:
3个灭活疫苗项目,全部由中国团队开发。
1个DNA基因疫苗,由美国Inovio公司开发,开发合作方包括北京的艾棣维欣/Advaccine生物制药。
2个信使分子RNA疫苗项目,包括Moderna公司项目,以及由BioNTech领衔、与复星医药和医药巨头辉瑞(Pfizer)合作的疫苗项目。
剩余两个项目均为非复制性载体疫苗,包括康希诺与军事科学院陈薇院士团队合作的项目,和牛津大学团队的项目。
8个疫苗项目都还没有进入三期临床。三期一般是临床试验的最后一个步骤,而根据病毒学、免疫学界人士介绍,大部分疫苗开发都是在二期实验结果不理想的情况下,没能进入临床三期就戛然而止。所以,临床二期结果完全公布之前,谨慎乐观。
Inovio牵头的DNA疫苗项目以及中科院武汉病毒研究所与国药集团合作研制的灭活病毒疫苗目前已经进入临床一期。北京生物制品的灭活病毒疫苗同时进行着临床的一期和二期实验。采用相似的一、二期并行以加快进度的还有牛津大学团队的腺病毒载体疫苗和BioNTech(复星、辉瑞协作支持)的RNA疫苗项目。
此外,科兴生物(Sinovac)5月10日发布消息称灭活病毒疫苗项目二期临床已经完成,预计7月份试生产;康希诺与军事科学院合作研发的腺病毒载体疫苗也接近完成。
△ Moderna官网
牛津团队对接了世界最大疫苗生产商
除了研发环节,疫苗的生产速度可能左右疫苗问世速度。一般在疫苗的临床实验结果清晰之前,制药厂商投产积极性不会太高。新冠疫情危机中,头部疫苗项目能否快速投产呢?
Moderna放出利好消息之前,牛津大学团队的腺病毒载体疫苗项目也被普遍看好,在北美和欧洲呼声极高。陈薇院士团队开发的疫苗虽同为腺病毒载体,不同之处在于源头是人体腺病毒,而牛津团队则采用了猕猴腺病毒为载体。预计截至五月底将有五千名志愿者参与二期、三期实验。
四月初牛津研制的载体疫苗(ChAdOx1A)在美国蒙大拿州的国立卫生研究所洛基山实验室进行了猕猴注射实验,结果乐观,刺激预热生产线的同时,牛津团队也表示疫苗有望在今年九月份问世。
从疫苗普及角度来看,牛津团队在科研推进的同时积累、对接了大量医药行业资源,攥紧了拳头蓄势待发。
合作伙伴包括:德国医药业巨头默克公司(Merck)、基因药物开发公司Oxford BioMedica 、由英国顶级学府合作成立并获得英国政府背书,致力于学术界与业界在疫苗研发和生产领域加快转化的疫苗生产与创新中心、总部在印度的世界最大疫苗生产商Serum Institute of India等等。
这个阵容列出来,除了法国赛诺菲和英国葛兰素史克两家公司单独开发一款疫苗(2020年底开始临床实验),欧洲的优质生物制药行业资源明显已经向牛津团队聚集。
一般来说,腺病毒重组作为载体的疫苗临床前研发快,免疫反应良好,主要的瓶颈可能是疫苗的生产周期。牛津团队的希尔教授认为需要搜寻量产上亿计疫苗的路径,这是印度疫苗产业的产能优势。
产能预热的流程里最重要的棋子其实是印度疫苗生产商 Serum。Serum公司CEO Adar Poonawalla在四月底跟牛津大学团队确定合作,并且会在疫苗尚未完成实验的情况下锁定生产线,今年九月份之前完成4000万支疫苗的生产。目前Serum每年的各类疫苗生产总量大约15亿,而印度是世界疫苗产业里的重要制造国,包括Serum在内的六家公司大约占世界所有疫苗年生产量的六成。
基因疫苗项目:政府背书,下一站提速
三个基因疫苗项目(DNA或RNA)也在悄然为量产预热。在美国“曲速计划”宣布之前,几个关键政府机构已经在过去几个月中相继为美国疫苗项目背书。
发家于美国的Inovio团队推出的是目前唯一一个“进入决赛”的DNA疫苗。目前Inovio在研发和实验层面主要是跟中国和韩国机构进行合作,生产合作除了德国的Richter-Helm之外几乎都是在于美国国内的合约生产方对接。
这个明显着眼美国国内的路径与开发资金的结构可能有关;除了得到关注公共卫生的盖茨基金会和国际性流行病应对机构CEPI的注资和背书,Inovio公司应用的智能注射装置CELLECTRA 3PSP在开发早期曾获得美国国防研究部门的八百万美金。但是先前Inovio对外承诺2020年底可以交付一百万剂量的疫苗,距离特朗普许下的三亿宏愿有相当距离。
Moderna同样有美国官方的背书。开发过程与美国国立哮喘与传染病研究院合作,并同时得到了CEPI以及美国生物制药高级研究开发署BARDA的资金支持。BARDA将支持Moderna最多4.83亿美元的资金用于加速相关疫苗的研发进程。
能得到BARDA支持与RNA疫苗的技术特点和生产提速潜力有关。新兴的RNA疫苗研制完成后,批量复制一段被小结构包裹的RNA要比传统方式生产速度快上许多。今年夏天启动的临床三期试验若可以验证疫苗在人体内能可靠激活人体免疫反应,对于以非药物手段控制疫情无望的美国来说,可快速生产的RNA疫苗才是雪中送炭。
另一个RNA疫苗项目由德国药企BioNTech领头,同时跟复星医药和美国医药巨头辉瑞(Pfizer)接触合作。虽然复星在三月中旬就同BioNTech接触,获得许可在中国独家开发和商业化开发中的疫苗产品,但关于BioNTech的最新疫苗进展都是与美国制药巨头辉瑞携手完成的。
辉瑞站队支持德方开发和上市后,对于在披露巨大开发成本受到资本市场认真审视的BioNTech来说是重大商业利好,等于安排好了制造、商业化和市场开拓的一条龙。5月13日,辉瑞CEO Bourla称目前已经在着手打通欧洲和美国的监管审批和量产渠道,希望在十月前后以“亿级”疫苗总量在欧洲和美国上市。
疫苗开发背后的拔河:国际合作 VS 国家利益
目前疫苗研发过程中,国际合作与国家利益是两股不完全相融的主导思路。
2017年达沃斯世界经济论坛上,流行病防范创新中心(CEPI)在盖茨基金会,英国最大慈善组织-惠康基金会以及挪威、日本、德国三国的4.6亿美金支持下成立,在世界范围内定向支持针对流行病的科研和疫苗开发。欧盟、澳大利亚、比利时、加拿大和英国也在2019年至今年3月间相继宣布注资,助力疫苗开发的国际合作。
CEPI是目前国际社会对疫苗开发资金支持力度最大的组织,也协调推动了相关国家各类药物开发和科学研究工作。8个进入临床阶段的新冠疫苗,有3个(INOVIO、牛津、Moderna)获得了联盟的资金支持。
4月底,世界卫生组织曾召集全世界各国领导人讨论国际社会形成合力共同开发新冠病毒针对性药物和疫苗,但是在法国、德国领导人高声疾呼的同时,中俄美印几大国缺席。并且,世界卫生组织召集会议时,特朗普宣布掐断美国对该国际组织的资金支持。
不跟国际社会协作,美国准备怎么做?
抛开特朗普的特立独行不谈,美国政府体系内已经把资源投入到了优质疫苗项目里了;美国国防研究部门,国立哮喘与传染病研究院,以及美国生物制药高级研究开发署(BARDA)支持、介入了DNA和RNA疫苗研发,而美国食品药品监督局也在五月初给Moderna公司RNA疫苗项目开了绿灯,快速批准了二期临床实验。
另一方面,美国政府已经和疫苗生产大国印度示好,美国务卿蓬佩奥四月中旬宣布会与印度成为携手开发新冠疫苗的伙伴。
中国在积极推进疫苗的国际合作,5月14日,康希诺生物和军事科学院的疫苗项目开始跟加拿大官方合作,推进疫苗在加拿大的临床试验。
昨天(5月18日)开幕的世卫大会上,国家主席习近平在致辞中宣布:中国将在两年内提供20亿美元国际援助,用于支持受疫情影响的国家特别是发展中国家抗疫斗争以及经济社会恢复发展;中国新冠疫苗研发完成并投入使用后,将作为全球公共产品,为实现疫苗在发展中国家的可及性和可担负性作出中国贡献。
疫苗研发的成本和收益
一款新冠病毒疫苗的研发过程,需要投入多少钱呢?
根据太平基金一份研报的分析,CEPI资助了一系列新冠病毒疫苗研发项目,到2021年计划投入22.75~27.75亿美元,目标是在2021年至少有3款候选疫苗提交上市申请,也就是说,如果把失败疫苗的成本也计算在内,那么对应每款成功上市的疫苗,平摊下来的研发成本在7.58~9.25亿美元。
投入如此高的研发费用,迎接一个不确定的未来,相关公司的股价却大涨,中美两家领跑的公司,康希诺今年上涨260%,Moderna上涨超过300%,这是为什么?
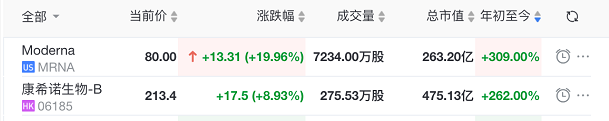
唯一的解释就是成功后的收益是巨大的,除了生命价值之外,经济回报也很高。
目前全球销售额第一的疫苗是辉瑞公司的沛儿——13价肺炎结合疫苗,2019年的销售额是58.47亿美元,新冠疫苗的市场空间远远超过这个数字。
按照太平基金研报的计算,如果要通过疫苗达到群体免疫,需要82.5%的人口接种疫苗,那么中国接种量需要达到11.55亿人,假设新冠疫苗国家免疫计划的价格60元/针,那么就相当于693亿元的市场空间。放到全球的话,这个空间就更大了。
当然,一将功成万骨枯。能走到最后的疫苗是少数,在它们通往成功的路上,躺着赔钱的是大多数。






















































